在中国,每年新发约88,200淋巴瘤患者中,非霍奇金淋巴瘤(NHL)约占所有淋巴瘤的91%,其中约66%为B细胞非霍奇金淋巴瘤,CLL或SLL约占所有B细胞非霍奇金淋巴瘤的6.4%,即每年新发患者约3,390例。MCL在所有B细胞非霍奇金淋巴瘤中约占5%,即每年新发患者约2,600多例。MCL患者一般预后较差,中位生存期为三至四年,并且患者在诊断时通常已经处于疾病晚期。
泽布替尼是百济神州自主研发的首个国产布鲁顿氏酪氨酸激酶(BTK)抑制剂。其通过优先审评、特殊审批方式于2020年6月3日被NMPA批准上市,并被纳入2020年医保目录,商品名“百悦泽”。
泽布替尼适应症:1)治疗复发/难治性(R/R)套细胞淋巴瘤(MCL)患者;2)治疗R/R慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL)患者。
泽布替尼,化学名称:(S)-7-[4-(1-丙烯酰基哌啶基)]-2-(4-苯氧基苯基)-4,5,6,7-四氢吡唑并[1,5-a]嘧啶-3-甲酰胺,化学式为:
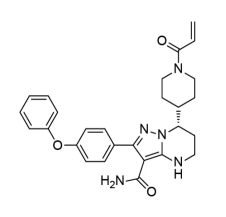
百济神州就泽布替尼在化合物、晶型和用途方面分别进行了重要专利布局:
泽布替尼的核心专利是化合物专利,即“作为蛋白质激酶抑制剂的稠合杂环化合物”(专利号:ZL201480003692.3),目前已进入了17个国家和地区,并已在中国、美国、欧洲、日本、韩国、加拿大等国家或地区获得授权。
晶型方面,CN109563099A保护了泽布替尼的一种晶型。
用途方面,CN110087680A保护在治疗癌症中的用途。WO2019108795A1保护治疗惰性或侵袭性B细胞淋巴瘤的用途。除此之外,CN104884458B、EP2989106B1均保护在制备用于治疗过敏性疾病、自身免疫性疾病、炎症疾病或癌症药物中的用途,US9447106B2为调节人体BTK激酶活性的方法以及治疗炎性疾病、类风湿性关节炎、B细胞增殖疾病的方法。
值得一提的是,目前,国内也有多家企业申报了BTK抑制剂新药,包括恒瑞医药、人福医药、浙江导明医药、艾森生物等多家药企,均申请了BTK靶向新药的临床试验,相信随着更多本土企业持续的研发投入,也会给BTK抑制剂发展和国内患者带来更多希望。

微信扫一扫
关注该公众号